Химические реакции в органической химии таблица. Реакции органических веществ. Классификация химических реакций по изменению степеней окисления химических элементов, образующих вещества
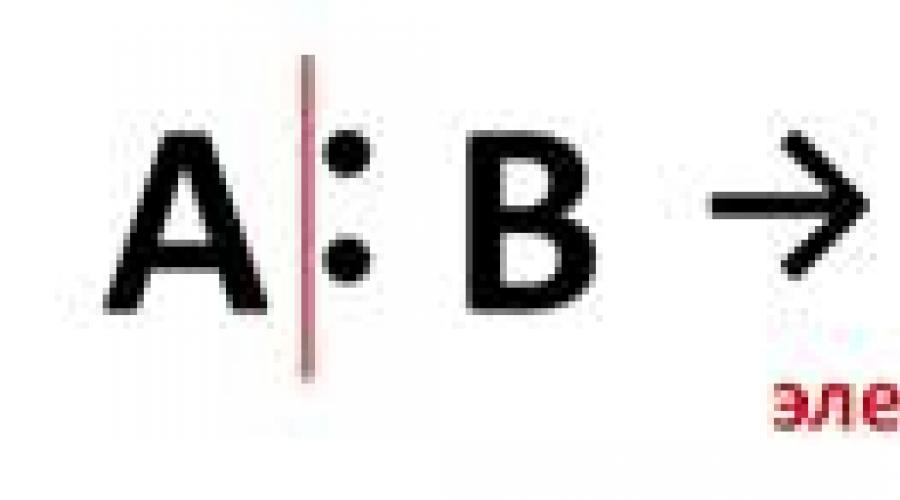
Читайте также
Занятие 2. Классификация реакций в органической химии. Упражнения на изомерию и гомологи
КЛАССИФИКАЦИЯ РЕАКЦИЙ В ОРГАНИЧЕСКОЙ ХИМИИ.
Существуют три основные классификации органических реакций.
1 Классификация по способу разрыва ковалентных связей в молекулах реагирующих веществ.
§ Реакции, протекающие по механизму свободнорадикального (гомолитического) разрыва связей. Такому разрыву подвергаются малополярные ковалентные связи. Образующиеся частицы называются свободными радикалами – хим. частица с неспаренным электроном, обладающая высокой химической активностью. Типичным примером такой реакции является галогенирование алканов, например :
§ Реакции, протекающие по механизму ионного (гетеролитического) разрыва связей. Такому разрыву подвергаются полярные ковалентные связи. В момент реакции образуются органические ионные частицы – карбкатион (ион, содержащий атом углерода с положительным зарядом) и карбанион (ион, содержащий атом углерода с отрицательным зарядом). Примером такой реакции может служить реакция гидрогалогенирования спиртов, например:
2. Классификация по механизму протекания реакции.
§ Реакции присоединения – реакция, в ходе которой из двух реагирующих молекул образуется одна (вступают непредельные или циклические соединения). В качестве примера приведите реакцию присоединения водорода к этилену:
§ Реакции замещения – реакция, в результате которой происходит обмен одного атома или группы атомов на другие группы или атомы. В качестве примера приведите реакцию взаимодействия метана с азотной кислотой:
§ Реакции отщепления (элиминирования) – отделение небольшой молекулы от исходного органического вещества. Выделяют a-элиминирование (отщепление происходит от одного и того же атома углерода, образуются неустойчивые соединения – карбены); b-элиминирование (отщепление происходит от двух соседних атомов углерода, образуются алкены и алкины); g-элиминирование (отщепление происходит от более удаленных атомов углерода, образуются циклоалканы). Приведите примеры вышеперечисленных реакций:
§ Реакции разложения – реакции, в результате которой из одной молекулы орг. соединения образуется несколько более простых. Типичным примером такой реакции служит крекинг бутана:
§ Реакции обмена – реакции, в процессе которых молекулы сложных реагентов обмениваются своими составными частями. В качестве примера приведите реакцию взаимодействия уксусной кислоты и гидроксида натрия:
§ Реакции циклизации – процесс образования циклической молекулы из одной или нескольких ациклических. Напишите реакцию получения циклогексана из гексана:
§ Реакции изомеризации – реакция перехода одного изомера в другой при определенных условиях. Приведите пример изомеризации бутана:
§ Реакции полимеризации – цепной процесс, последовательное соединение низкомолекулярных молекул в более крупные высокомолекулярные путем присоединения мономера к активному центру, находящемуся на конце растущей цепи. Полимеризация не сопровождается образованием побочных продуктов. Типичным примером является реакция образования полиэтилена:
§ Реакции поликонденсации – последовательное соединение мономеров в полимер, сопровождающееся образованием низкомолекулярных побочных продуктов (воды, аммиака, галогеноводорода и т.д.). В качестве примера напишите реакцию образования фенолформальдегидной смолы:
§ Реакции окисления
а) полное окисление (горение), например:
б) неполное окисление (возможно окисление кислородом воздуха или сильными окислителями в растворе – KMnO 4 , K 2 Cr 2 O 7). В качестве примера запишите реакции каталитического окисления метана кислородом воздуха и варианты окисления этилена в растворах с разным значением рН:
3. Классификация по химизму реакции.
· Реакция галогенирования – введение в молекулу орг. соединения атома галогена путем замещения или присоединения (заместительное или присоединительное галогенирование). Напишите реакции галогенирования этана и этена:
· Реакция гидрогалогенирования – присоединение галогеноводородов к непредельным соединениям. Реакционная способность возрастает с увеличением молярной массы Hhal. В случае ионного механизма реакции присоединение идет по правилу Марковникова: ион водорода присоединяется к наиболее гидрогенизированному атому углерода. Приведите пример реакции взаимодействия пропена и хлороводорода:
· Реакция гидратации – присоединение воды к исходному органическому соединению, подчиняется правилу Марковникова. В качестве примера запишите реакцию гидратации пропена:
· Реакция гидрирования – присоединение водорода к органическому соединению. Обычно проводят в присутствии металлов VIII группы Периодической системы (платина, палладий) в качестве катализаторов. Напишите реакцию гидрирования ацетилена:
· Реакция дегалогенирования – отщепление атома галогена от молекулы орг. соединения. В качестве примера приведите реакцию получения бутена-2 из 2,3-дихлорбутана:
· Реакция дегидрогалогенирования – отщепление молекулы галогеноводорода от органической молекулы с образованием кратной связи или цикла. Обычно подчиняется правилу Зайцева: водород отщепляется от наименее гидрогенизированного атома углерода. Запишите реакцию взаимодействия 2-хлорбутана со спиртовым раствором гидроксида калия:
· Реакция дегидратации – отщепление молекулы воды от одной или нескольких молекул орг. вещества (внутримолекулярная и межмолекулярная дегидратация). Осуществляется при высокой температуре или в присутствии водоотнимающих средств (конц. H 2 SO 4 , P 2 O 5). Приведите примеры дегидратации этилового спирта:
· Реакция дегидрирования – отщепление молекулы водорода от орг. соединения. Напишите реакцию дегидрирования этилена:
· Реакция гидролиза – обменная реакция между веществом и водой. Т.к. гидролиз в большинстве случаев обратим, его проводят в присутствии веществ, связывающих продукты реакции, или удаляют продукты из сферы реакции. Гидролиз ускоряется в кислой или щелочной среде. Приведите примеры водного и щелочного (омыление) гидролиза этилового эфира уксусной кислоты:
· Реакция этерификации – образование сложного эфира из органической или неорганической кислородсодержащей кислоты и спирта. В качестве катализатора применяют конц. серную или соляную кислоты. Процесс этерификации обратим, поэтому продукты необходимо удалять из сферы реакции. Запишите реакции этерификации этилового спирта с муравьиной и с азотной кислотами:
· Реакция нитрования – введение группы –NO 2 в молекулы орг. соединений, например реакция нитрования бензола:
· Реакция сульфирования – введение группы –SO 3 Н в молекулы орг. соединений. Запишите реакцию сульфирования метана:
· Реакция алкилирования – введение радикала в молекулы орг. соединений вследствие реакций обмена или присоединения. В качестве примера запишите реакции взаимодействия бензола с хлорэтаном и с этиленом:
Упражнения на изомерию и гомологи
1. Укажите, какие из следующих веществ являются гомологами по отношению друг к другу: С 2 Н 4 , С 4 Н 10 , С 3 Н 6 , С 6 Н 14 , С 6 Н 6 , С 6 Н 12 , С 7 Н 12 , С 5 Н 12 , С 2 Н 2 .
2. Составьте структурные формулы и дайте названия всем изомерам состава С 4 Н 10 О (7 изомеров).
3. Продукты полного сгорания 6,72л смеси этана и его гомолога, имеющего на один атом углерода больше, обработали избытком известковой воды, при этом образовалось 80г осадка. Какого гомолога в исходной смеси было больше? Определите состав исходной смеси газов. (2,24л этана и 4,48л пропана).
4. Составьте структурную формулу алкана с относительной плотностью паров по водороду 50, в молекуле которого имеется по одному третичному и четвертичному атому углерода.
5. Среди предложенных веществ выделите изомеры и составьте их структурные формулы: 2,2,3,3,-тетраметилбутан; н-гептан; 3-этилгексан; 2,2,4-триметилгексан; 3-метил-3-этилпентан.
6. Вычислите плотность паров по воздуху, по водороду и по азоту пятого члена гомологического ряда алкадиенов (2,345; 34; 2,43).
7. Напишите структурные формулы всех алканов, содержащих 82,76% углерода и 17,24% водорода по массе.
8. На полное гидрирование 2,8г этиленового углеводорода израсходовали 0,896л водорода (н.у.). Определите углеводород, если известно, что он имеет неразветвленное строение.
9. При добавлении какого газа к смеси равных объемов пропана и пентана ее относительная плотность по кислороду увеличится; уменьшится?
10. Приведите формулу простого газообразного вещества, имеющего такую же плотность по воздуху, как простейший алкен.
11. Составьте структурные формулы и назовите все углеводороды, содержащие 32е в молекуле 5 изомеров).
Реакции органических веществ можно формально разделить на четыре основных типа: замещения, присоединения, отщепления (элиминирования) и перегруппировки (изомеризации) . Очевидно, что все многообразие реакций органических соединений невозможно свести к предложенной классификации (например, реакции горения). Однако такая классификация поможет установить аналогии с уже знакомыми вам реакциями, протекающими между неорганическими веществами.
Как правило, основное органическое соединение, участвующее в реакции, называют субстратом , а другой компонент реакции условно рассматривают как реагент .
Реакции замещения
Реакции замещения - это реакции, в результате которых осуществляется замена одного атома или группы атомов в исходной молекуле (субстрате) на другие атомы или группы атомов.
В реакции замещения вступают предельные и ароматические соединения, такие как алканы, циклоалканы или арены. Приведем примеры таких реакций.
Под действием света атомы водорода в молекуле метана способны замещаться на атомы галогена, например, на атомы хлора:
Другим примером замещения водорода на галоген является превращение бензола в бромбензол:

Уравнение этой реакции может быть записано иначе:
![]()
При этой форме записи реагенты, катализатор, условия проведения реакции записывают над стрелкой, а неорганические продукты реакции - под ней.
В результате реакций замещения у органических веществ образуются не простое и сложное вещества, как в неорганической химии, а два сложных вещества.
Реакции присоединения
Реакции присоединения - это реакции, в результате которых две или более молекул реагирующих веществ соединяются в одну.
В реакции присоединения вступают ненасыщенные соединения, такие как алкены или алкины. В зависимости от того, какая молекула выступает в качестве реагента, различают гидрирование (или восстановление), галогенирование, гидрогалогенирование, гидратацию и другие реакции присоединения. Каждая из них требует определенных условий.
1.Гидрирование - реакция присоединения молекулы водорода по кратной связи:
2. Гидрогалогенирование - реакция присоединения галогенводорода (гидрохлорирование):
3. Галогенирование - реакция присоединения галогена:
![]()
4.Полимеризация - особый тип реакций присоединения, в ходе которых молекулы вещества с небольшой молекулярной массой соединяются друг с другом с образованием молекул вещества с очень высокой молекулярной массой - макромолекул.
Реакции полимеризации - это процессы соединения множества молекул низкомолекулярного вещества (мономера) в крупные молекулы (макромолекулы) полимера.
Примером реакции полимеризации может служить получение полиэтилена из этилена (этена) под действием ультрафиолетового излучения и радикального инициатора полимеразации R.
Наиболее характерная для органических соединений ковалентная связь образуется при перекрывании атомных орбиталей и образовании общих электронных пар. В результате этого образуется общая для двух атомов орбиталь, на которой находится общая электронная пара. При разрыве связи судьба этих общих электронов может быть разной.
Типы реакционноспособных частиц
Орбиталь с неспаренным электроном, принадлежащая одному атому, может перекрываться с орбиталью другого атома, на которой также находится неспаренный электрон. При этом происходит образование ковалентной связи по обменному механизму:
Обменный механизм образования ковалентной связи реализуется в том случае, если общая электронная пара образуется из неспаренных электронов, принадлежащих разным атомам.
Процессом, противоположным образованию ковалентной связи по обменному механизму, является разрыв связи, при котором к каждому атому отходит по одному электрону (). В результате этого образуются две незаряженные частицы, имеющие неспаренные электроны:
![]()
Такие частицы называются свободными радикалами.
Свободные радикалы - атомы или группы атомов, имеющие неспаренные электроны.
Свободнорадикальные реакции - это реакции, которые протекают под действием и при участии свободных радикалов.
В курсе неорганической химии это реакции взаимодействия водорода с кислородом, галогенами, реакции горения. Реакции этого типа отличаются высокой скоростью, выделением большого количества тепла.
Ковалентная связь может образоваться и по донорно-акцепторному механизму. Одна из орбиталей атома (или аниона), на которой находится неподеленная электронная пара, перекрывается с незаполненной орбиталью другого атома (или катиона), имеющего незаполненную орбиталь, при этом формируется ковалентная связь, например:
![]()
Разрыв ковалентной связи приводит к образованию положительно и отрицательно заряженных частиц (); так как в данном случае оба электрона из общей электронной пары остаются при одном из атомов, у другого атома получается незаполненная орбиталь:
![]()
Рассмотрим электролитическую диссоциацию кислот:
![]()
Можно легко догадаться, что частица, имеющая неподеленную электронную пару R: — , т. е. отрицательно заряженный ион, будет притягиваться к положительно заряженным атомам или к атомам, на которых существует по крайней мере частичный или эффективный положительный заряд.
Частицы с неподеленными электронными парами называют нуклеофильными агентами
(nucleus
- «ядро», положительно заряженная часть атома), т. е. «друзьями» ядра, положительного заряда.
Нуклеофилы (Nu ) - анионы или молекулы, имеющие неподеленную пару электронов, взаимодействующие с участками молекул, на которых сосредоточен эффективный положительный заряд.
Примеры нуклеофилов: Сl — (хлорид-ион), ОН — (гидроксид-анион), СН 3 O — (метоксид-анион), СН 3 СОО — (ацетат-анион).
Частицы, имеющие незаполненную орбиталь, напротив, будут стремиться заполнить ее и, следовательно, будут притягиваться к участкам молекул, на которых присутствует повышенная электронная плотность, отрицательный заряд, неподеленная электронная пара. Они являются электрофилами, «друзьями» электрона, отрицательного заряда или частиц с повышенной электронной плотностью.
Электрофилы - катионы или молекулы, имеющие незаполненную электронную орбиталь, стремящиеся к заполнению ее электронами, так как это приводит к более выгодной электронной конфигурации атома.
Электрофилом с незаполненной орбиталью является не любая частица. Так, например, катионы щелочных металлов имеют конфигурацию инертных газов и не стремятся к приобретению электронов, так как имеют низкое сродство к электрону.
Из этого можно сделать вывод, что несмотря на наличие у них незаполненной орбитали, подобные частицы не будут являться электрофилами.
Основные механизмы протекания реакций
Выделено три основных типа реагирующих частиц - свободные радикалы, электрофилы, нуклеофилы - и три соответствующих им типа механизма реакций:
- свободнорадикальные;
- электрофильные;
- нулеофильные.
Кроме классификации реакций по типу реагирующих частиц, в органической химии различают четыре вида реакций по принципу изменения состава молекул: присоединения, замещения, отщепления, или элиминирования (от англ. to eliminate - удалять, отщеплять) и перегруппировки. Так как присоединение и замещение могут происходить под действием всех трех типов реакционноспособных частиц, можно выделить несколько основных механизмов протекания реакций.


Кроме того, рассмотрим реакции отщепления, или элиминирования, которые идут под воздействием нуклеофильных частиц - оснований.
6. Элиминирование:
Отличительной чертой алкенов (непредельных углеводородов) является способность вступать в реакции присоединения. Большинство этих реакций протекает по механизму электрофильного присоединения.
Гидрогалогенирование (присоединение галоген водорода):
При присоединении галогенводорода к алкену водород присоединяется к более гидрированному атому углерода, т. е. атому, при котором находится больше атомов водорода, а галоген - к менее гидрированному .
CH 3 -CH 3 + Cl 2 – (hv) ---- CH 3 -CH 2 Cl + HCl
C 6 H 5 CH 3 + Cl 2 --- 500 C --- C 6 H 5 CH 2 Cl + HCl
Реакции присоединеия
Такие реакции характерны для органических соединений, содержащих кратные(двойные или тройные) связи. К реакциям этого типа относятся реакции присоединения галогенов, галогеноводородов и воды к алкенам и алкинам
CH 3 -CH=CH 2 + HCl ---- CH 3 -CH(Cl)-CH 3
Реакции отщепления (элиминирования)
Это реакции, приводящие к образованию кратных связей. При отщеплении галогеноводородов и воды наблюдается определенная селективность реакции, описываемая правилом Зайцева, согласно которому атом водорода отщепляется от того атома углерода, при котором находится меньше атомов водорода. Пример реакции
CH3-CH(Cl)-CH 2 -CH 3 + KOH →CH 3 -CH=CH-CH 3 + HCl
Полимеризации и поликонденсации
n(CH 2 =CHCl) (-CH 2 -CHCl)n
Окислительно-восстановительные
Наиболее интенсивная из окислительных реакций – это горение, реакция, характерная для всех классов органических соединений. При этом в зависимости от условий горения углерод окисляется до С (сажа), СО или СО 2 , а водород превращается в воду. Однако для химиков-органиков большой интерес представляют реакции окисления, проводимые в гораздо более мягких условиях, чем горение. Используемые окислители: растворы Br2 в воде или Cl2 в CCl 4 ; KMnO 4 в воде или разбавленной кислоте; оксид меди; свежеосажденные гидроксиды серебра (I) или меди(II).
3C 2 H 2 + 8KMnO 4 +4H 2 O→3HOOC-COOH + 8MnO 2 + 8KOH
Этерификации (и обратной ей реакции гидролиза)
R 1 COOH + HOR 2 H+ R 1 COOR 2 + H 2 O
Циклоприсоединение
Y R Y-R
‖ + ‖ → ǀ ǀ
R Y R-Y
‖ + →
11. Классификация органических реакций по механизму. Примеры.
Механизм реакции предполагает детальное постадийное описание химических реакций. При этом устанавливают, какие именно ковалентные связи разрываются, в каком порядке и каким путем. Столь же тщательно описывают образование новых связей в процессе реакции. Рассматривая механизм реакции, прежде всего обращают внимание на способ разрыва ковалентной связи в реагирующей молекуле. Таких способов два – гомолитический и гетеролитический.
Радикальные реакции протекают путем гомолитического (радикального) разрыва ковалентной связи:

Радикальному разрыву подвергаются неполярные или малополярные ковалентные связи (С–С, N–N, С–Н) при высокой температуре или под действием света. Углерод в радикале СН 3 имеет 7 внешних электронов (вместо устойчивой октетной оболочки в СН 4). Радикалы неустойчивы, они стремятся захватить недостающий электрон (до пары или до октета). Один из способов образования устойчивых продуктов – димеризация (соединение двух радикалов):
СН 3 + СН 3 СН 3 : СН 3 ,
Н + Н Н : Н.
Радикальные реакции – это, например, реакции хлорирования, бромирования и нитрования алканов:

Ионные реакции протекают с гетеролитическим разрывом связи. При этом промежуточно образуются короткоживущие органические ионы – карбкатионы и карбанионы – с зарядом на атоме углерода. В ионных реакциях связывающая электронная пара не разъединяется, а целиком переходит к одному из атомов, превращая его в анион:

К гетеролитическому разрыву склонны сильно полярные (Н–O, С–О) и легко поляризуемые (С–Вr, С–I) связи.
Различают нуклеофильные реакции (нуклеофил – ищущий ядро, место с недостатком электронов) и электрофильные реакции (электрофил – ищущий электроны). Утверждение, что та или иная реакция является нуклеофильной или электрофильной, условно всегда относится к реагенту. Реагент – участвующее в реакции вещество с более простой структурой. Субстрат – исходное вещество с более сложной структурой. Уходящая группа – это замещаемый ион, который был связан с углеродом. Продукт реакции – новое углеродсодержащее вещество (записывается в правой части уравнения реакции).
К нуклеофильным реагентам (нуклеофилам) относят отрицательно заряженные ионы, соединения с неподеленными парами электронов, соединения с двойными углерод-углеродными связями. К электрофильным реагентам (электрофилам) относят положительно заряженные ионы, соединения с незаполненными электронными оболочками (АlCl 3 , ВF 3 , FeCl 3), cоединения с карбонильными группами, галогены. Электрофилы – любые атом, молекула или ион, способные присоединить пару электронов в процессе образования новой связи. Движущая сила ионных реакций – взаимодействие противоположно заряженных ионов или фрагментов разных молекул с частичным зарядом (+ и –).
В ходе реакции в молекулах реагирующих веществ разрываются одни химические связи и образуются другие. Органические реакции классифицируются по типу разрыва химических связей в реагирующих частицах. Из их числа можно выделить две большие группы реакций - радикальные и ионные.
Радикальные реакции - это процессы, идущие с гомолитическим разрывом ковалентной связи. При гомолитическом разрыве пара электронов, образующая связь, делится таким образом, что каждая из образующихся частиц получает по одному электрону. В результате гомолитического разрыва образуются свободные радикалы:
Нейтральный атом или частица с неспаренным электроном называется свободным радикалом.
Ионные реакции - это процессы, идущие с гетеролитическим разрывом ковалентных связей, когда оба электрона связи остаются с одной из ранее связанных частиц:
В результате гетеролитического разрыва связи получаются заряженные частицы: нуклеофильная и электрофильная.
Нуклеофильная частица (нуклеофил) - это частица, имеющая пару электронов на внешнем электронном уровне. За счет пары электронов нуклеофил способен образовывать новую ковалентную связь.
Электрофильная частица (электрофил) - это частица, имеющая незаполненный внешний электронный уровень. Электрофил представляет незаполненные, вакантные орбитали для образования ковалентной связи за счет электронов той частицы, с которой он взаимодействует.
В органической химии все структурные изменения рассматриваются относительно атома (или атомов) углерода, участвующего в реакции.
В соответствии с вышеизложенным хлорирование метана под действием света классифицируют как радикальное замещение, присоединение галогенов к алкенам - как электрофильное присоединение, а гидролиз алкилгалогенидов - как нуклеофильное замещение.
Наиболее часто встречаются следующие типы оеакций.
Основные типы химических реакций
I. Реакции замещения (замена одного или нескольких атомов водорода на атомы галогенов или спецгруппу) RCH 2 X + Y → RCH 2 Y + X
II. Реакции присоединения RCH=CH 2 + XY → RCHX−CH 2 Y
III. Реакции отщепления (элиминирования) RCHX−CH 2 Y → RCH=CH 2 + XY
IV. Реакции изомеризации (перегруппировки)
V. Реакции окисления (взаимодействие с кислородом воздуха или окислителя)
В этих вышеперечисленных типах реакции различают ещё и специализированные и именные реакции.
Специализированные:
1) гидрирование (взаимодействие с водородом)
2) дегидрирование (отщепление от молекулы водорода)
3) галогенирование (взаимодействие с галогеном: F 2 , Cl 2 , Br 2 , I 2)
4) дегалогенирование (отщепление от молекулы галогена)
5) гидрогалогенирование (взаимодействие с галогенводородом)
6) дегидрогалогенирование (отщепление от молекулы галогенводорода)
7) гидратация (взаимодействие с водой в необратимой реакции)
8) дегидратация (отщепление от молекулы воды)
9) гидролиз (взаимодействие с водой в обратимой реакции)
10) полимеризация (получение многократного увеличенного углеродного скелета из одинаковых простых соединений)
11) поликонденсация (получение многократного увеличенного углеродного скелета из двух разных соединений)
12) сульфирование (взаимодействие с серной кислотой)
13) нитрование (взаимодействие с азотной кислотой)
14) крекинг (уменьшение углеродного скелета)
15) пиролиз (разложение сложных органических веществ на более простые под действием высоких температур)
16) реакция алкилирования (введение в формулу радикала алкана)
17) реакция ацилирования (введение в формулу группы –C(CH 3)O)
18) реакция ароматизации (образование углеводорода ряда аренов)
19) реакция декарбоксилирования (отщепление от молекулы карбоксильной группы -COOH)
20) реакция этерификации (взаимодействие спирта с кислотой, или получение сложного эфира из спирта или карбоновой кислоты)
21) реакция «серебряного зеркала» (взаимодействие с аммиачным раствором оксида серебра (I))
Именные реакции:
1) реакция Вюрца (удлинение углеродного скелета при взаимодействии галогенпроизводного углеводорода с активным металлом)
2) реакция Кучерова (получение альдегида при взаимодействии ацетилена с водой)
3) реакция Коновалова (взаимодействие алкана с разбавленной азотной кислотой)
4) реакция Вагнера (окисление углеводородов с двойной связью кислородом окислителя в слабощелочной или нейтральной среде при нормальных условиях)
5) реакция Лебедева (дегидрирование и дегидратация спиртов при получении алкадиенов)
6) реакция Фриделя-Крафтса (реакция алкилирования арена хлоралканом при получении гомологов бензола)
7) реакция Зелинского (получение бензола из циклогексана дегидрированием)
8) реакция Кирхгофа (превращение крахмала в глюкозу при каталитическом действии серной кислоты)